既存薬で寿命を延ばせる可能性
人工妊娠中絶薬のミフェプリストンという薬があります。
最近の研究で、この薬に寿命を延ばす可能性があるかもしれないということが分かってきました。

もともと線虫において、ミフェブリストンによる寿命延長の効果が確認されていましたが、今回、西カリフォルニア大学の研究チームがミフェプリストンを投与することで、ショウジョウバエの寿命が延びることを発見しました。
交尾の際、メスのショウジョウバエはオスからセックスペプチドと呼ばれる分子を受け取ります。これまでの研究では、セックスペプチドが炎症を引き起こし、雌のハエの健康や寿命を縮めることがわかっていました。
今回、研究チームは交尾した雌のショウジョウバエにミフェブリストンを与えると、セックスペプチドの作用がブロックされ、炎症を抑えて健康を維持し、薬剤を受け取らなかった場合よりも寿命が長くなることを発見しました。
さらに研究チームは、ミフェプリストンがどのようにして寿命を延ばすのかをより深く理解しようと、ショウジョウバエがミフェプリストンを摂取したときに変化する遺伝子、分子、代謝プロセスを調べました。その結果、若年性ホルモンと呼ばれる分子が中心的な役割を果たしていることが分かりました。さらに特筆すべきは、これらの代謝経路は、人間で保存されているということです。
今回この研究を行ったジョンタワー教授は
「線虫とショウジョウバエは進化的にかなり離れた動物であり、共通して寿命延長の効果が見られたことに大きな意義があります。人間に対しても同じ効果があるかもしれません」と述べています。
参考文献: Scientists may have found one path to a longer life
こうした研究のようにすでに存在する薬が、寿命の延長に効果があるかもしれないという話題はとても面白いです。
糖尿病治療薬のメトホルミンでも、マウスの実験で寿命延長の効果が報告されています。
こうした既存の治療薬のメリットは、すでに販売されているため、安全性が一定以上担保されている点です。もし、人間にも同様に寿命延長の効果があると分かった場合、広く大衆に薬を供給するなどのハードルもかなり低くなることでしょう。
一方でデメリットとしては、こうした寿命に良いという情報が一人歩きしてしまい、勝手に服用をはじめる人が増えてしまわないかという点です。いくら、臨床試験を合格した薬剤であるとはいえ、もちろん副作用はあります。処方には医師による適切な判断が不可欠です。また、本当にこの薬が必要である患者さんに供給されなくなってしまっては、本末転倒です。そもそもまだ人間での効果は立証されていません。
私たちは科学的エビデンスに基づいて、しっかりと適切な判断をしていかねばならないのだと改めて感じました。
ポンプ機能を持った人工心臓の開発に成功
世界では年間で1700万人以上の方が心臓病で亡くなっています。
これを防ぐためには、心臓の移植手術が必要ですが、ドナーの方の数も足りておらず、深刻な問題となっています。
そんな中。バイオ3Dプリンターを用いた人工心臓の開発が進展しています!
ミネソタ大学の研究チームがバイオ3Dプリンターを用いて、ヒトの細胞由来の心臓ポンプを作成することに成功しました。この研究チームでは、長年人工心臓の開発に取り組んでいました。今までのアプローチは幹細胞を心筋細胞に分化させてから、心臓に組み込むという方法でしたが、これでは上手くポンプ機能を再現するのに失敗してきました。そこで新たなアプローチとして、幹細胞を人工心臓に組み込んだ後に、それを心筋細胞に分化させるという方法をとりました。
その結果、今回は初めてポンプの機能を有した心筋細胞の集合体を形成できまたとのことです。
イントロ
心臓の幾何学的に複雑な構造を再現したモデルでは、軟質の生体材料を用いて、心臓のチャンバーや大血管を収容することができ、3Dバイオプリンティングを用いて再現することが可能である。しかし、ポンプ機能をサポートするために連続した生きた筋肉を組み込むことは、まだ達成されていなかった。これは主に、非増殖性の細胞タイプであることで有名な心筋細胞を高密度で収容しなければならないという課題に起因している。一方で、別の方法としては、高密度に増殖して組織空間を埋めることができるヒト誘導多能性幹細胞を用いて印刷し、その後、その場で心筋細胞に分化させることが考えられていた。
本研究では、ヒト多能性幹細胞の増殖と心筋細胞への分化を促進するバイオインクを開発し、連続する心筋で構成された電気機械的に機能するチャンバー型オルガノイドを 3 次元的にプリントする。
方法と結果
このバイオインクを用いて、2 つのチャンバーと血管の入口と出口を備えたヒト人工多能性幹細胞を搭載した構造体を 3 次元的に印刷した。ヒト多能性幹細胞を十分な密度まで増殖させた後、構造体内で細胞を分化させ、得られたヒトチャンバー型筋ポンプの機能を実証した。ヒトチャンバー型筋ポンプは、マクロスケールの拍動と、薬物やペーシングへの応答性を伴う連続的な活動電位の伝播を実証した。接続されたチャンバーは、灌流を可能にし、心臓の機能や健康や疾患に伴うリモデリングの研究に不可欠な圧力/容積関係の再現を可能にした。
結論
この進歩は、心筋のポンプ機能に不可欠な幾何学的構造を有するという重要な利点を持ちながら、集合体ベースのオルガノイドに似たマクロスケールの組織の生成に向けた重要な一歩を踏み出したものである。将来的には、このタイプのヒトチャンバー型オルガノイドは、心臓医療機器の治験としての役割を果たし、最終的には治療用組織移植につながる可能性がある。
参考文献
https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.119.316155
感想
現在はまだ約1.5cmの小さな構造体ということですが、今後サイズを大きくしていき、人間のサイズの心臓を作ることができる日もそう遠くはないでしょう。
文献でも述べらている通り、この人工心臓開発技術は、心臓移植の手段として有用であることはもちろんのこと、薬の効き目を測定するための治験用としての利用可能性もあることでしょう。
バイオ3Dプリンターの技術を使った研究は、医療を大きく変えるブレイクスルーになる可能性があるので、引き続き注目分野です!
バイオ3Dプリンターに関する以前の記事はこちら
ハイドロゲルで何歳になっても歩ける世界へ
老化によって生じるさまざまな症状の一つに、膝の悩みがあります。
健康寿命を延ばし、寝たきりを防ぐためにもいつまでも健康に歩けることはとても重要です。
今回はそんな膝の悩みが解決できるかもしれない、ハイドロゲルの開発の最前線をご紹介します。
私たちが一歩踏み出すたびに、膝には体重の約2倍の負担がかかります。軟骨は長年にわたる膨大な量の圧力に耐えることができますが、治癒や修復の能力には限界があります。長年の摩耗や損傷は治療が難しく、多くの患者さんは人工膝関節の手術を10年~15年に一度受けなければなりませんでした。
そこで、人工膝関節の代替として、科学者たちはハイドロゲルに注目して、研究を行ってきました。
人間の軟骨は、何十年にもわたる激しい消耗にも耐えられるほどの強度をもっています。しかしその一方で、膝を動かすのに十分なほど柔らかくて繊細な性質を持っています。ハイドロゲルは柔らかさは持っており、軟骨の代替として最適でしたが、強度の面で問題を抱えており、実用化は未だされていませんでした。
しかし今回、デューク大学の研究者たちはがヒトの軟骨に匹敵する強度を持ったハイドロゲルを開発し、大きな業績をあげています。
デューク大学のベン・ワイリーとケン・ガルの研究チームがヒトの軟骨にかなり近いハイドロゲルの作成に成功しました。このハイドロゲルは60%が水分であるにも関わらず、強い強度を誇ります。写真のように100ポンドのケトルベルの重さにも、形を失ったり、損傷を受けたりすることなく耐えることができました。

また、オーストラリア国立大学の研究チームでは、自己修復能力を持ったハイドロゲルについても開発しています。
こうしたハイドロゲルの開発によって、高齢者の膝の悩みが解決できる未来になることが期待されています。
参考文献
Magical hydrogel mimics cartilage to promote healthspan - Longevity.Technology
関連リンク
【第1回】バイオベンチャーのビジネスモデル ~バイオベンチャーと製薬会社~
バイオベンチャーが儲かる仕組みについて知りたいというご意見が多かったので、今回から数回に分けて、バイオベンチャーのビジネスモデルについて解説していきたいと思います。
今回はまず、臨床試験の仕組みとバイオベンチャーが果たす役割について取り上げていきます。

まずは、創薬の流れについて解説しておきます。
まず非臨床試験として、マウスなどを用いた動物実験が行われます。
この非臨床試験をクリアできた場合、臨床試験に進むことができます。
臨床試験では、3段階の試験(Phase1~3)があります。この3段階の試験をクリアするのがけっこう大変で、よく治験の失敗で株価が連日ストップ安になるなんてバイオベンチャーも見かけます。
ちなみに試験の成功確率が一番低いのがPhase2試験です。
既存の薬と同じ効果ではダメで、既存の薬よりも良いということを示すのが大変だからです。
※抗がん剤などの副作用が強い薬の場合は、健康な被験者への投与は省き、Phase1から患者さんに投与して安全性を確かめている例もあります。
臨床試験をすべてクリアできたら、行政機関に薬としての認可をもらうための申請を行います。日本であれば厚生労働省、アメリカであればFDAに提出します。
そして、行政機関からの承認が得られれば、新薬として発売することができます。
非臨床試験から販売までの一連のプロセスは、だいたい10年程度はかかる長い道のりです。

さて、こうした創薬の過程で、バイオベンチャーと大手製薬会社では役割分担がされています。
バイオベンチャーは薬の候補となる化合物を見つけてくるところに強みを持っています。
一方で、大手製薬会社はスムーズに臨床試験を進めて、新薬を販売することに強みを持っています。
従って、開発段階が進んでいく中で、両者は協力関係を結ぶことになるのです。
次回は実際にお金がどのように動いているか、バイオベンチャーの財政事情を取り上げていこうと思います。
Brd2阻害による老化の防止
マウスの寿命がわずかに伸びたことを示す研究は数多くあります。
その代表例となっているのが、カロリー制限です。介入によってマウスの食事量が減ると、たとえそのカロリー制限が適度な毒性を持っていたとしても、長生きする傾向があることが分かっています。
短命種において、カロリー制限によってもたらされる健康と寿命の改善はとても大きなものであることが示されています。こうしたカロリー制限と寿命に関する研究は非常に多くされています。
しかし、種の本来の寿命が長ければ長いほど、カロリー制限による延命の効果も小さくなることが分かってきており、カロリー制限がマウスの場合と同じようにヒトでも、大きな寿命延長の効果につながるとは期待されていません。
そうした中で、本日ご紹介するのは、老化研究の分野ではない研究者が偶然発見したものです。てんかんに関連する遺伝子Brd2が、長寿に関連する多くの細胞プロセスに関係していることが判明しました。

老化は分子や細胞の損傷の累積的な影響によるものと考えられていますが、私たちはてんかんの研究のために開発したBrd2ハプロ不全(Brd2+/-、以下HET)マウスモデルが、野生型(Brd2+/+、以下WT)マウスに比べて寿命が大幅に長いことを偶然に発見しました。ブロモドメイン(BET)タンパク質であるBRD2がてんかんの素因となるメカニズムを追求したところ、あからさまに正常なHETマウスは、野生型マウスに比べて寿命が大幅に長いだけでなく、がんの発生率の低下や腎機能の改善など、健康的な老化表現型を示すことがわかりました。
マウスの長寿に影響を与える遺伝子や分子過程はいくつか知られていましたが、これらの遺伝子の多くは、Brd2の影響を受けていることが分かりました。
例えば、カロリー制限マウスではIGFシグナルが減少することが知られていましたが、これと同様にBrd2ハプロ不全はIGFシグナルをダウンレギュレーションします。
また、サーチュイン経路のアップレギュレーションは寿命の延長と関連していますが、Brd2ハプロ不全はサーチュイン経路の遺伝子をアップレギュレーションしていました。具体的には、サーチュイン1(SIRT1)とそのホモログは、DNA修復、ゲノム安定性、炎症、アポトーシス、細胞周期進行、ミトコンドリア呼吸などの長寿に関連するプロセスを制御しています。Brd2の発現が低下すると、酸化ストレスを減少させる機能を持った、p53、Nqo1、Hmox1の発現が増加しました。さらに、p53のアップレギュレーションは、ゲノムの安定性を高め、DNA修復を促進し、寿命を延ばす効果もあります。Brd2のハプロ不全は、長寿に関連する複数の遺伝子や分子過程と関連しているため、Brd2の発現低下は、寿命に影響を与える基本的な(遺伝的な)因子である可能性があります。
細胞レベルだけでなく、個体レベルでの効果も観察されました。Brd2はプロ不全(Brd2+/-)マウスでは、野生型動物(Brd2+/+)と比較して寿命が23%延長し、癌の発生率が43%減少しました。さらに、Brd2ハプロ不全マウスは、同年齢の野生型マウスと比較して、グルーミング(毛繕い)の改善、受胎期間の延長、加齢による腎機能や形態の悪化の抑制などが観察されました。これらのデータは、Brd2のハプロ不全が老化の改善の役割を担っていることを示唆しています。我々は、Brd2が分子や細胞の損傷の蓄積を防ぐことで老化に影響を与えているのではないかと仮説を立てています。BET阻害剤の開発における最近の進歩を考えると、我々の研究は、加齢に関連する疾患を理解し、治療・予防する方法として、BRD2を標的とする薬剤を検討するためのきっかけとなることでしょう。
参考文献
感想
最近の老化研究の傾向として、今回のケースのように別分野での研究が、たまたま老化研究につながったというケースが多いかと思います。たしか、カロリー制限と寿命との関係の発見も、最初は別分野の研究の副産物だった気がします。こうした点からも、老化研究の分野はまだまだ未成熟であり、潜在可能性の大きな分野であると言えるでしょう。
さて、BRD2をはじめとしたBETブロモドメインについては、これを標的とした阻害剤については、抗がん剤として研究されてきましたが、最近ではてんかん治療薬として有用である可能性も出てきました。筆者らもてんかん治療薬としての可能性を研究している途中で、老化との関連を発見したようです。とても面白い研究成果だと思うので、これから引き続き注目していきたいと思います。
小さなロボットが手術を変える!?
テック分野の開発はバイオに負けず劣らず目覚ましいものがあります。
そしてこうした技術は、上手くいけば医療にも応用できるかもしれません。
今回は医療への応用の可能性が高そうな技術である、マイクロロボットについて取り上げていきます。
参考 https://www.seas.harvard.edu/news/2020/06/next-generation-cockroach-inspired-robot-small-mighty

ハーバード大学などの研究チームが、とても小さなロボットを開発しました。その大きさは写真の通り、コインほどであります(長さ約2cm、重さ約0.3g)。
これまでこのサイズのロボットでは、前進・後進などの単純な動きしかできず、複雑な動きはできませんでした。
しかし今回のロボットは、昆虫の動きをアイデアの着眼としており、動作の自由度は高いとのことです。2次元シートの組み合わせでできており、制作も比較的簡単のようです。

今回の論文の共著者であるロバート・ウッド氏は、「この新しいロボットによって、折り畳みベースの組み立てアプローチによって、複雑なロボットでも小さく設計できることを示すことができた」と述べています。
こうしたマイクロロボットが将来、どんどん小さくなっていき、注射によって体内に微小な手術用ロボットを注入できるような時代が来るかもしれません。
また、以前ご紹介した生体ロボットなどと組み合わせると、さらに面白い展開があるかもしれません。
感想
近年、生命科学はいろいろな分野とつながり始めています。遺伝子解析における情報科学の導入はその最たる例と言えるでしょう。これからは、今回ご紹介したようなテックの分野との結びつきも盛んになっていくでしょうし、領域を超えた技術の結びつきがさらなるイノベーションを起こすと考えています。
こうした、イノベーションを起こすには、やはり大局的な視点から技術と技術の組み合わせを提案できるような存在が必要であり、VCがそうした役割を担っていくべきであると私は考えています。
免疫が作る未来 ~バイオベンチャー紹介 vol.2 KOTAI~
今回は、大阪大学の研究技術が基になったKOTAIという会社をご紹介します。
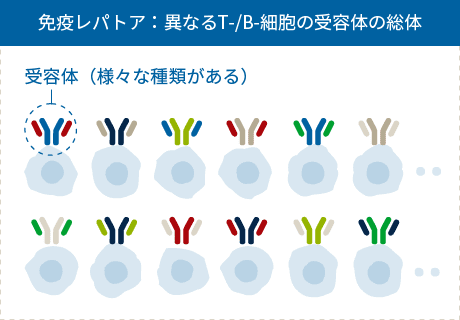
リンパ球を構成する、T細胞、B細胞はその表面に抗原認識分子であるT/B細胞受容体(TCR/BCR)を発現しています。何か抗原に出会うと免疫記憶によって1度出会った抗原を記憶しておくことができるという性質を持っています。そして、この抗原をバイオマーカーとして測定してしまえば、リンパ球がいまどういう応答に備えているのかが分かり、病気の診断や薬剤の有効性の予測に使えるのではないかと言われてきました。
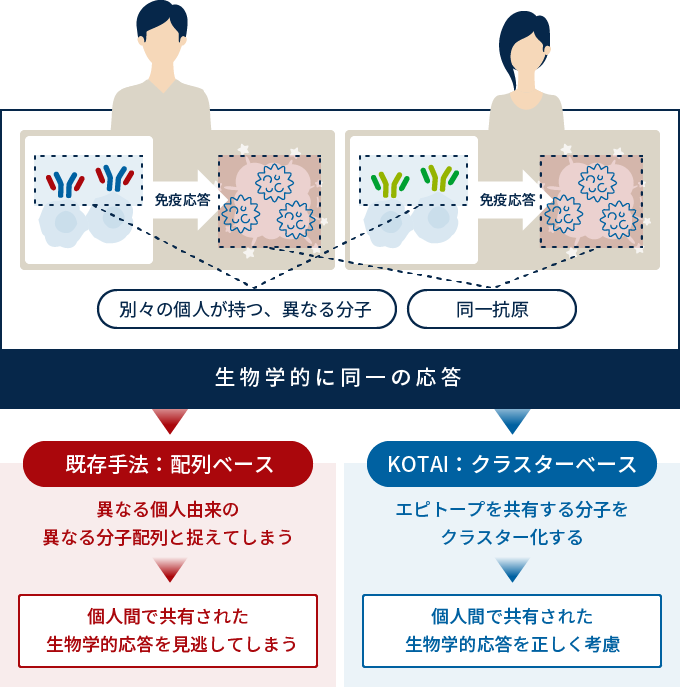
しかしここには大きな問題がありました。まず一つ目は遺伝子の多様性の問題です。T/B細胞受容体は遺伝子配列によって(10の12乗)通りの組み合わせがあります。2つ目は配列が個人間で共有されていないという点です。上の図のように、受容体の遺伝子の組み合わせが個人間で異なっていても同じ反応をするということが分かっていました。
そのため、誰かの配列を参考にバイオマーカーを作っても他の人には役立たないという問題点がありました。
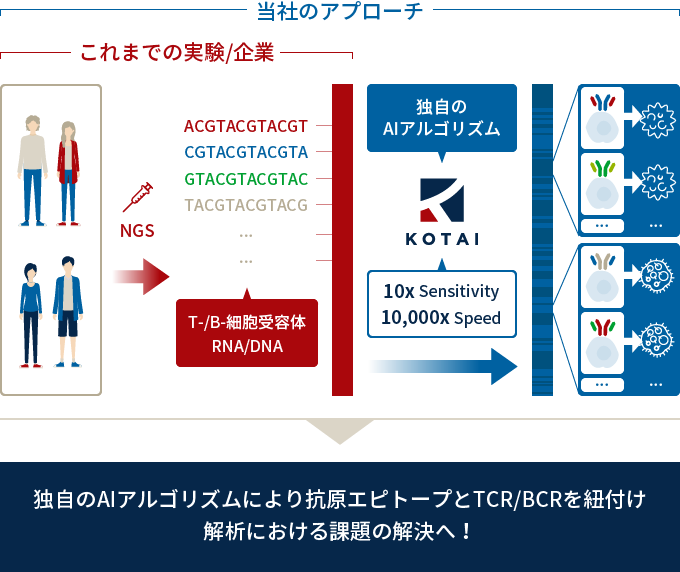
これを解決するのがKOTAIの技術です。AIによる解析によってT/B細胞受容体の配列を分析し、その抗体を予測することで、バイオマーカーを確立しようという試みです。

同社は、2016年に設立された新しい会社ですが、東京大学や国立がん研究所など有力な研究機関と提携を行っています。

なお、RNA-seq等の受託サービスも行っています。おそらくそうした受託サービスを収益源としながら自社の研究開発費に充てているものと推測されます。


